ה־FDA הודיע השבוע באופן רשמי שניסוי קליני יחיד יהפוך לברירת המחדל באישור תרופות, גם כאלה שמיועדות לשווקים גדולים. זהו אחד משינויי המדיניות הדרמטיים ביותר שהוביל ה־FDA בשנים האחרונות. מאז שנות ה־90 של המאה ה־20, הרשות דורשת בדרך כלל ניסוי יעילות ראשוני (שלב II), ואחריו שני ניסויים קליניים גדולים (שני שלבי III).
● זריקת ההרזיה דור 2 של נובו נורדיסק נכשלה בניסוי השוואתי מול מונג'ארו
● אל תגלו לרוג'ר ווטרס: מה מצאו חוקרים בטכניון על הלהיט של פינק פלויד?
זהו נוהל ולא חוק, ובשנים האחרונות כבר היו כמה יוצאי דופן. תרופות יתום המיועדות לשווקים קטנים מאוד, או תרופות שה־FDA הגדיר "דחופות", זכו להקלות, אך שני ניסויים גדולים היו הסטנדרט.
להחלטה הזאת יש השלכות על השוק כולו, וגם על חברות ישראליות.
דרך חדשה להשיג מידע
בניגוד לחלק מההחלטות של ראש ה־FDA מרטי מקארי ושל ראש תחום המוצרים הביולוגיים והחיסונים ויניי פרסאד, שזכו לביקורת נוקבת, הפעם השוק מוצא בה היגיון, גם אם יש לה חסרונות.
לדברי איל ליפשיץ, שותף בקרן הון הסיכון הישראלית פרגרין, "ההגדרה החדשה אומרת שהאישור הוא על בסיס ניסוי יעילות גדול אחד, בתוספת מידע תומך. עם השנים, הצטברו דרכים חדשות להעריך רעילות ויעילות של תרופות על בסיס מודלים ביולוגיים חדשים, מודלים סטטיסטיים חדשים וסמנים ביולוגיים. הניסויים לא יכללו בהכרח מספר קטן יותר של נבדקים בהשוואה למה שהיה מקובל עד היום, אלא הניסוי היחיד יהיה גדול יחסית, כך שהמוצר ייבדק על אותו מספר אנשים כבעבר, לפני שמשחררים אותו לשוק".
אך מבחינת יעילות, הסטטיסטיקה בנויה כך שהצלחה בניסוי קליני אחד יכולה, לעתים רחוקות, להתרחש במקרה, גם אם המוצר אינו יעיל.
"זה נכון, ולשם כך ממשיכים לאסוף מידע גם אחרי האישור. מהפכת המידע יצרה אפשרויות חדשות גם בתחום הזה".
מטרת השינוי היא להביא תרופות חדשות במהירות רבה יותר לשוק, להוזיל את תהליך הפיתוח, ובסופו של דבר להוזיל כתוצאה מכך את מחירי התרופות. ייתכן שהצעד גם ימשוך משקיעים, שהמסלול הארוך והיקר מהמעבדה לשוק הרתיע אותם.
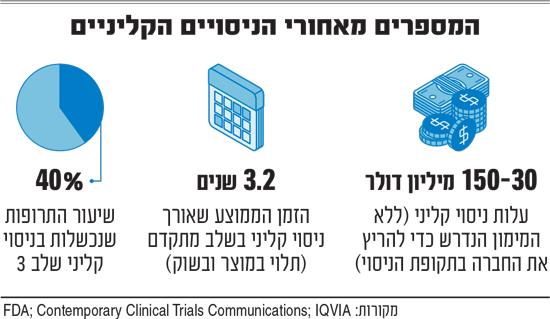
ניסוי קליני עולה 30־150 מיליון דולר, וזאת בלי להביא בחשבון את המימון הנדרש להחזקת החברה לאורך תקופת הניסוי שעשוי להגיע לעשרות מיליוני דולרים.
כמות על חשבון איכות
במאמר שפרסמו השבוע מקארי ופרסד בכתב העת The New England Journal of Medicine, הם טוענים שכיום, בניגוד לעבר, רוב התרופות שמגיעות לאישור ה־FDA מגובות בהבנה מנגנונית עמוקה, ולכן הסיכוי שיתברר שהן לא עובדות בשלב III הוא נמוך.

מרטי מקארי, ראש ה־FDA, מנהל המזון והתרופות / צילום: Reuters, Elizabeth Frantz
הטענה הזאת נתפסה עד היום כקריאה אופטימית של המציאות, נוכח העובדה ש־40% מהניסויים הקליניים בשלב III נכשלים, באופן שמפתיע את כל מי שהשקיע את כספו ואת נשמתו במוצרים הללו. מעבר לכך, גם במוצרים רבים שברור שהם יעילים, אנחנו עדיין חוקרים מדוע בכלל הם יעילים. לדוגמה, האקמול, שכתבנו עליו בעבר.
עם זאת, אם להפחתת מספר הניסויים אכן תתלווה הקפדה מוגברת על קבלת מידע על מנגנון הפעילות של התרופות, ייתכן ששיעורי ההצלחה שלהן בניסוי האחד שיידרש מהן יהיו גבוהים יותר.
מקארי ופרסאד טענו גם שעד כה ה־FDA נטה להסתמך יותר מדי מנגנון שני הניסויים, על חשבון איכות הניסוי. הם אומרים שעדיין ניתן יהיה להסתמך על שני ניסויים, במקרים ספציפיים שבהם ניסוי אחד ייתפס כלא מספיק (למשל באותם מקרים שבהם נראה כי מוצר עובד, אך המנגנון לא ברור ורוצים לוודא שתוצאת הניסוי אינה מקרית).
אין יותר מקום לטעויות
ליפשיץ אופטימי לגבי השפעת השינוי על חברות ישראליות. "הפחתת עלויות הפיתוח הנובעת מהמהלך עשויה להכניס חברות ישראליות רבות יותר למשחק. אנחנו כבר נערכים לבצע את השינוי, ולמשל חברת הפורטפוליו שלנו לוטריס פארמה, מתחום הסרטן, תיערך כעת לביצוע ניסוי יחיד. לפני כן לא ידענו כמה ניסויים נצטרך".
ד"ר ג'רמי לוין, בעבר מנכ"ל חברת טבע ובעל ניסיון עשיר בניהול ניסויים קלינים, בעיקר בתחומי הסרטן והנוירולוגיה, חושש מטעויות שעלולות חברות צעירות בכלל, וישראליות בפרט, לעשות מול הרגולציה החדשה.
"חברות ישראליות יחשבו שהרגולציה הזאת הופכת את החיים שלהן לקלים יותר. ואכן, יש פה הזדמנות להפחית עלויות וזמני פיתוח, וזה חשוב מאוד לחברות הישראליות שעבורן הנגישות להון ומחיר ההון לרוב גבוהים מעבור חברות אמריקאיות. עם זאת, אם הרגולציה הזו תבוצע כפי שנאמר, היא תחליף את הדרישה לשני ניסויים, בדרישה לניסוי אחד שהוא כל כך חזק, וכל כך נתמך במידע משלים, עד שניסוי נוסף כמעט לא יוסיף ערך.
"זה אומר תהליך קצר יותר, אבל גם כזה שאין בו מקום לטעויות. ואם התוצאה לא חזקה, או שמשהו בניסוי לא נראה ל־FDA - לא בחרתם יעד עיקרי מדויק לניסוי, השמטתם יותר מדי חולים, שיניתם את הפרוטוקול באמצע, או שההבדל שנמצא בין הקבוצות הוא גבולי - אין הזדמנות נוספת.
"חברות ישראליות שאינן מנוסות מספיק ויתייחסו לשינוי כקיצור דרך - יכשילו את עצמן. בעקבות השינוי, הדרישה למצוינות ולקפדנות מתחילת הדרך דווקא גוברת, והגישה הישראלית של 'נצא לדרך ואז נראה, נתקן תוך כדי תנועה' - אתם צריכים לשכוח מזה בעולם פיתוח התרופות.
"הקשר עם ה־FDA, שהוא מורכב עבור חלק מהחברות הישראליות, הצורך להבין עד הסוף מה המנהל רוצה - אלה דברים שיהפכו חשובים עוד יותר מבעבר. יזמים ישראלים, בעיקר ככל שהחברות צעירות יותר, לפעמים חושבים שהם יודעים יותר טוב, שיהיה בסדר. זו גישה חשובה לרוח היזמות הישראלית אבל עכשיו יותר מתמיד, צריך להשאיר אותה מחוץ לדלת ה־FDA, ורק להקשיב ולוודא שהבנתם איזה ניסוי הוא באמת רוצה".
תמרור אזהרה נוסף מציב ללוין ליזמי הייטק, שבשנים האחרונות נכנסים יותר לפיתוח תרופות. "יזמי ההייטק רגילים לכך שהמהירות משיגה ניצחון", אומר לוין, "אבל לא, בתרופות תכנון מוקדם מעמיק משיג ניצחון. אתם רגילים לכך שהמוצר הכי טוב מנצח. לא, בעולם התרופות גוף הראיות הטוב ביותר מנצח. ועכשיו, אין לכם הזדמנות שנייה ללמוד זאת".
לתשומת לבכם: מערכת גלובס חותרת לשיח מגוון, ענייני ומכבד בהתאם ל
קוד האתי
המופיע
בדו"ח האמון
לפיו אנו פועלים. ביטויי אלימות, גזענות, הסתה או כל שיח בלתי הולם אחר מסוננים בצורה
אוטומטית ולא יפורסמו באתר.