מנכ"לית חברת התרופות כן פייט , פרופ' פנינה פישמן, טוענת כי למוצר של החברה לטיפול בדלקת מפרקים "יש את מה שדרוש" לביצוע עסקת מסחור. המוצר כבר מוסחר לשוק היפני בעסקה שבה קיבלה כן פייט 7.5 מיליון דולר, ועשויה עוד לקבל 20 מיליון דולר בתשלומי אבני דרך ו-12% בתמלוגים.
"יפן מהווה כ-10% מהשוק העולמי למחלה, ולכן אנו מקווים לחתום על עסקה שתהיה לפחות גדולה פי 10 מהעסקה היפנית", אמרה פישמן, וציינה כי היא מקווה שזה יקרה עד סוף השנה.
פישמן אמרה את הדברים בכנס של חברת קשרי המשקיעים גלברט כהנא, בו השתתפו ארבע חברות דואליות.
לכן פייט העדפה ברורה לא לקחת את המוצר לבדה לשלב הבא של הניסויים בדלקת מפרקים, שכן הניסוי אמור להיות גדול ויקר. עם זאת, היא כבר פועלת בעצמה לתכנן את פרוטוקול הניסוי ולקבל עבורו אישור מהרשויות.
אבני דרך נוספות להן מצפה החברה השנה הן: קבלת תוצאות של ניסוי שלב II/III בפסוריאזיס ברבעון הרביעי; תוצאות מניסוי שלב II בגלאוקומה הנערך על ידי החברה הבת אופתליקס; וכניסה לשלב II במוצר לטיפול בסרטן הכבד. פישמן רמזה ל"דברים טובים" שיגיעו מכיוון הבת אופתליקס בקרוב, וזאת לאחר כישלון צורב בתרופה שפיתחה זו על בסיס הטכנולוגיה של כן פייט, לתחום העין היבשה.
פישמן מציינת כי את 2013 סיימה החברה עם 6 מיליון דולר בקופתה, וגייסה 5 מיליון דולר נוספים, ואלו על פי התוכנית שהוצגה יספיקו לחברה עד סוף 2015, לכן לא צפוי גיוס בקרוב.
רדהיל: נכנסים לניסוי באינדיקציה נוספת במוצר ה-102
חברת רדהיל הגיעה לכנס לאחר שכבר חתמה על עסקת מסחור מפתיעה עבור אחד המוצרים הפחות מדוברים שלה, תרופה לריקון המעי לפני קולונוסקופיה. מנכ"ל החברה, דרור בן אשר, ציין כי בדיקת הנאותות למוצר על ידי חברת salix נמשכה כשנתיים. בסופן נרכשו זכויות המסחור ב-7 מיליון דולר באופן מיידי, לצד תשלומי אבני דרך של 5 מיליון דולר ותמלוגים חד ספרתיים.
המוצר המוביל של החברה היום מבחינת השלב בפיתוח הוא ה-RHB103, לטיפול במיגרנה. התרופה כבר הוגשה לשיווק בארה"ב, והתקבלו שאלות מטעם רשות המזון והתרופות האמריקאית (FDA). בן אשר מדגיש כי השאלות היו מינוריות, לא דנו בבטיחות ויעילות המוצר, אלא בעיקר בתהליך הייצור על ידי צד שלישי המייצר את חומרי הגלם של החברה, "אבל שום דבר ספציפי או מדאיג", לדבריו. החברה נערכת לביצוע ניסוי נוסף, לשם אישור המוצר גם מול רשויות הרגולציה האירופיות.
מוצר ה-102 של רדהיל למניעת בחילות והקאות, סיים ניסויים קליניים ונמצא גם הוא בתהליכי הגשה ל-FDA, והחידוש הוא שהפך לאחד המוצרים המרכזיים של החברה, לאחר שגילתה כי הוא עשוי להתאים להתוויה חדשה. בכוונת החברה להיכנס לניסוי שלב III במוצר לאותה התוויה חדשה, שאת טיבה היא אינה חושפת עדיין.
מלבדו, שני המוצרים המובילים של החברה הם התרופות האנטיביוטיות למחלת קרוהן ונגד חיידק H Pylori - RHB104ו-105 בהתאמה. המוצר לקרוהן הוא ההימור הגדול של רדהיל והניסוי היקר ביותר שלה. הוא הצליח בעבר בניסוי שלב II באוסטרליה, אך נכשל כשנוסה על ידי חברת פייזר. לדברי בן אשר, "פייזר, עם כל היותה ענקית פארמה, פשוט טעתה באופן ביצוע הניסוי וניתוח התוצאות. הניתוח מחדש שלהן על ידי צד שלישי השיג תוצאות טובות דווקא, ואפילו הופיע בכתב העת המדעי המוביל Lancet".
ה-105 משתמש באותו קוקטייל אנטיביוטי לטיפול בחיידק הידוע כגורם לאולקוס, ההופך בהדרגה עמיד לתרופות האנטיביוטיות הנהוגות כיום. תוצאות ניסוי שלב III במוצר זה צפויות ברבעון השלישי השנה.
פלוריסטם: ניסוי שלב III בקוריאה על חשבון השותפה המקומית
זמי אברמן, מנכ"ל חברת תאי הגזע פלוריסטם , הסביר כי הוא רואה בתחום תאי הגזע את הגל הבא של הביוטכנולוגיה. "בפיתוח תרופות קלאסי מסנתזים אותן במעבדה, ובביוטכנולוגיה, שהייתה הגל השני של פיתוח תרופות, מייצרים את החומרים בתאים חיים, ואז מזקקים ומזריקים אותם", ציין. "בשיטה שלנו, מזריקים את התאים החיים והם מפרישים את החומרים הרצויים בגוף. זה צעד נוסף באותו הכיוון".
לחברה מספר מוצרים בצנרת לחסימות כלי דם בגפיים, שיקום שריר, טיפול בלחץ דם בריאות וטיפול לרעלת הריון. יתרונות התאים של פלוריסטם הם, על פי אברמן, היכולת להזריקם מספר פעמים בלי ליצור תגובה של מערכת החיסון, וכן שרידותם הגבוהה בגוף. בחיות נמצא כי התאים שורדים ארבעה שבועות; בבני אדם קשה למדוד, אך הערכת החברה היא כי התא צריך לשרוד בגוף האדם יותר מאשר בחיה.
במהלך השנה אמורה החברה להתחיל ניסוי שלב III בקוריאה על חשבון השותפה הקוריאנית שלה, Cha, בהתוויה של חסימה מלאה של כלי דם. הגיוס לניסוי שלב II בחסימות חלקיות אמור להסתיים עד סוף השנה, וכשישה חודשים לאחר מכן יהיה אפשר להתחיל בניתוח התוצאות. אברמן דווקא נלהב ביותר מהמוצר של החברה לרעלת הריון, שהשיג עד כה רק תוצאות פרה-קליניות טובות, אך עשוי להתקדם מהר כיוון שזו מחלה שאין לה כל תרופה.
פרוטליקס: "הפעילות בברזיל כבר מתבטאת בדוח הרבעוני"
דוד אביעזר, מנכ"ל חברת פרוטליקס , אמר כי "עד התקופה הזו בשנה הבאה, נהיה עם שני מוצרים נוספים בניסויי שלב III", בנוסף למוצר שהחברה כבר משווקת, למחלה הנדירה גושה.
אחד מהם הוא הטיפול במחלת פברי, מחלה גנטית נדירה, שנמצא בשלב II והתוצאות הסופיות צפויות במחצית השנייה של 2014. השני הוא מוצר חדש לטיפול בגושה הניתן בבליעה ולא בעירוי. היתרון של המוצר אינו רק בנוחות לחולה, אלא בכך שבניגוד לעירוי אותו נהוג לתת בקצב של פעם בשבועיים, את הכדור ניתן לתת אחת ליום, וכך ליצור רמה אחידה יותר של האנזים בדם שאמורה להוביל לשיפור בבריאות.
באשר למוצר המוביל של החברה לגושה, שחדירתו לארה"ב נחוותה על ידי המשקיעים כמאכזבת במקצת, אמר אביעזר כי פעילות בשווקים נוספים כמו ברזיל וצ'ילה, תתבטא כבר בדוחותיה הקרובים. "פייזר, השותפה שלנו לשיווק המוצר, עשתה כמה שינויים מבניים בחברה, שהדגישו את הפעילות של יחידת התרופות למחלות נדירות שאליה אנחנו שייכים", אומר אביעזר. הוא מקווה כי המהלך ייתן דחיפה קדימה למהלכי השיווק של פייזר סביב המוצר, בין היתר לפלח הילדים, עבורו היא אמורה לקבל אישור בארה"ב בקרוב.
המשקיעים עדיין זוכרים לכם שטרם האישור, נסחרתם בשווי גבוה יותר אפילו מאשר היום.
אביעזר: "גם אני זוכר את זה. שווי יכול להשתנות מהר מאוד. לא כל כך נהנינו מהעליות בשוק הביומד, ועכשיו אנחנו מתגלגלים עם כולם בירידות. אבל בין המשקיעים שלנו יש מוסדיים רבים חזקים, כולל קרנות עילית אמריקאיות, והם יודעים שביוטק זה סיפור לטווח ארוך".
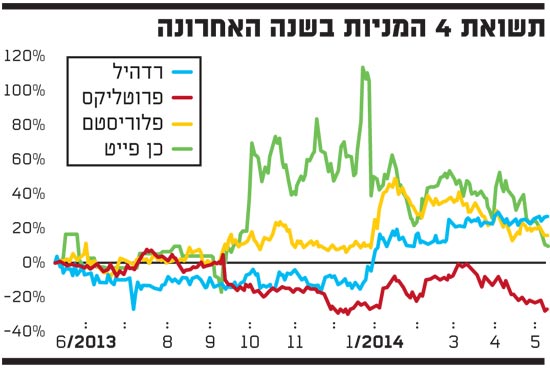
תשואת 4 המניות מתחילת השנה
לתשומת לבכם: מערכת גלובס חותרת לשיח מגוון, ענייני ומכבד בהתאם ל
קוד האתי
המופיע
בדו"ח האמון
לפיו אנו פועלים. ביטויי אלימות, גזענות, הסתה או כל שיח בלתי הולם אחר מסוננים בצורה
אוטומטית ולא יפורסמו באתר.